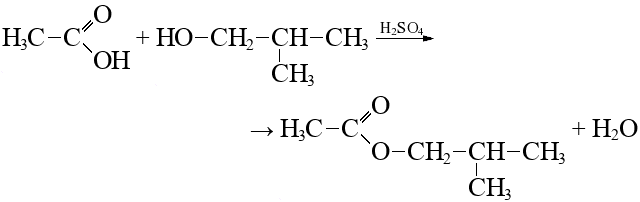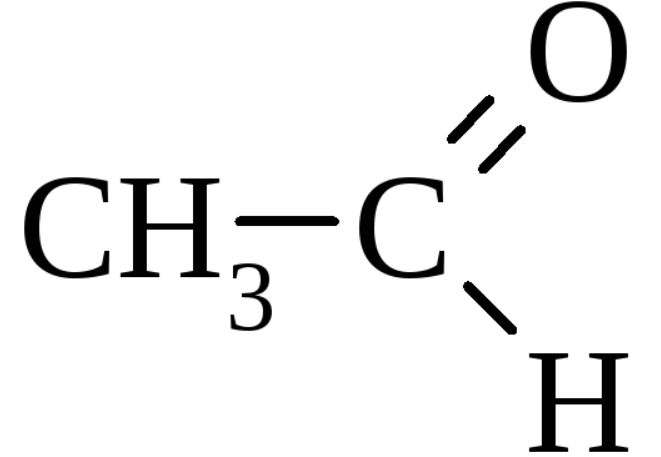Уксусная кислота (этановая кислота, химическая формула C2H4O2 или CH3COOH, AcOH) - слабая органическая кислота, относящаяся к классу предельных карбоновых кислот. Узнайте свойства, состав и применение уксуса в пищевой промышленности, кулинарии и других отраслях.
Cодержание
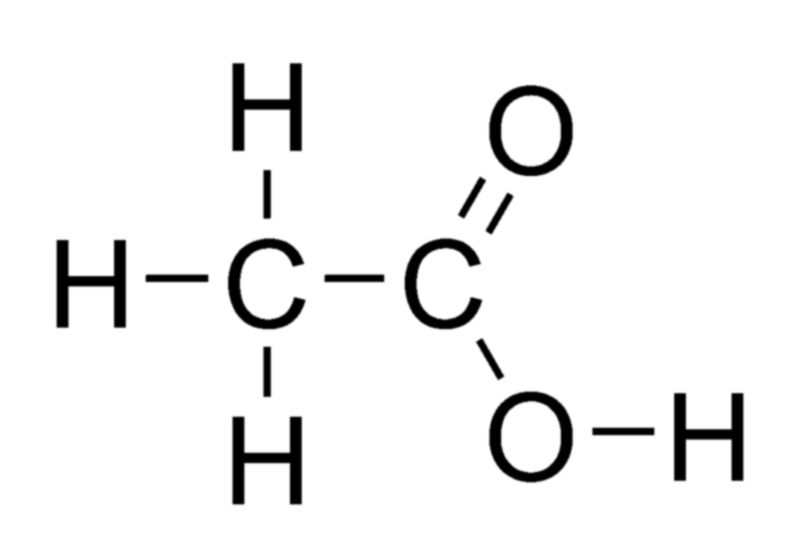
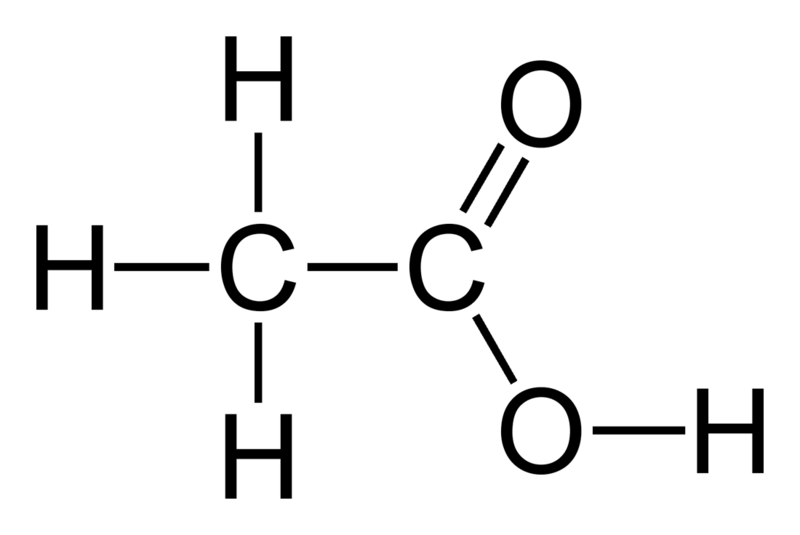
У́ксусная кислота́ (эта́новая кислота, химическая формула — C2H4O2 или CH3COOH, AcOH) — cлабая органическая кислота, относящаяся к классу предельных карбоновых кислот.
Свойства и состав
Уксусная кислота при стандартных условиях является одноосновной карбоновой кислотой, представляющей собой бесцветную жидкость с характерным резким запахом и кислым вкусом. Ее химическая формула CH3COOH указывает на присутствие уксусного остатка (CH3COO-) и ионов водорода (H+).
Натуральный уксус, также известный как столовый уксус, содержит помимо уксусной кислоты и другие пищевые кислоты, такие как лимонная, виннокаменная, яблочная и др. Также в составе уксуса присутствуют альдегиды, сложные эфиры, сложные спирты, которые придают уксусу его аромат и букет.
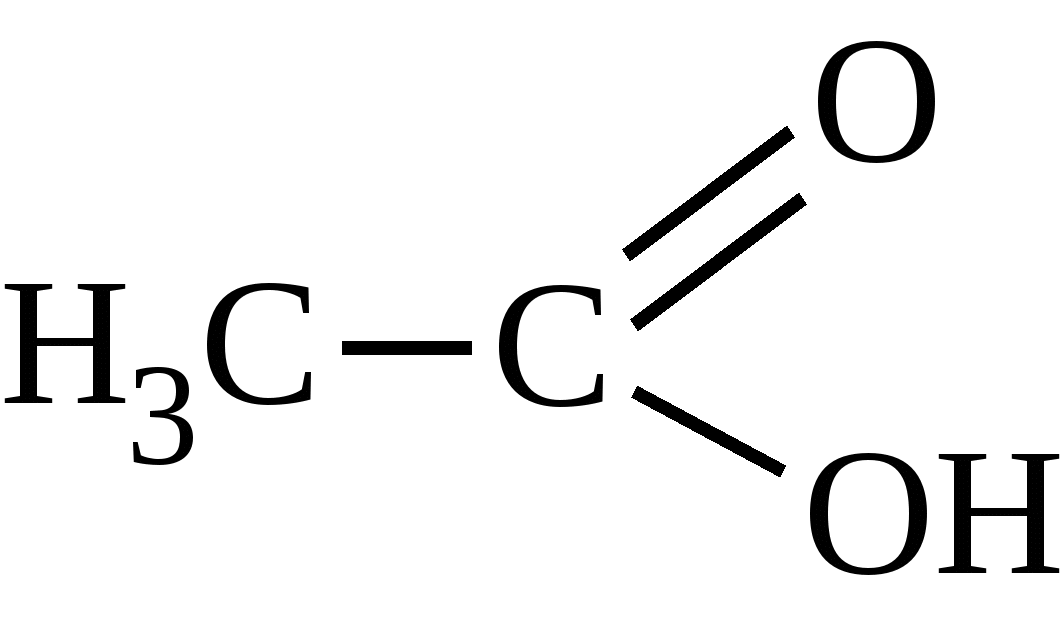
История
Уксус известен человеку с древних времен. Первые упоминания о его применении относятся к III веку до н.э., когда греческий ученый Теофраст описал его действие на металлы, приводящее к образованию пигментов, используемых в искусстве. Уксус также использовался для получения свинцовых белил и ярь-медянки. В Древнем Риме готовили специально прокисшее вино, известное как "сапа", которое содержало большое количество ацетата свинца. Однако, такое употребление сапы привело к хроническому отравлению свинцом среди римской аристократии.
В VIII веке арабский алхимик Джабир ибн Хайян описал способы получения уксуса, а во времена Эпохи Возрождения его получали путем возгонки ацетатов металлов. В 1847 году немецкий химик Адольф Кольбе синтезировал уксусную кислоту из неорганических материалов, что открыло новые возможности для ее производства.
См. также
Производство
Столовый уксус получают разбавлением водой уксусной эссенции, которая содержит около 80% пищевой уксусной кислоты. Уксусная эссенция получается уксуснокислым брожением жидкостей, содержащих этиловый спирт, с помощью уксуснокислых бактерий в аэробной среде. После брожения производится очистка, пастеризация, разбавление и розлив уксуса.
Синтетическая уксусная кислота производится путем химического синтеза из природного газа или при сухой перегонке древесины. В России около 50 заводов производят уксус, из которых 10-15 производят натуральный уксус. Однако, потребность в уксусе не покрывается текущим производством, поэтому значительная часть уксуса в России импортируется.
Применение
Столовый уксус, также известный как пищевой уксус, применяется в кулинарии в качестве приправы и консерванта. Он представляет собой 3—15%-й водный раствор пищевой уксусной кислоты.
Соли и сложные эфиры уксусной кислоты называются ацетатами. Ацетат натрия, получаемый в результате реакции между уксусной кислотой и содой, является растворимой в воде пищевой добавкой и используется как консервант.

Биохимические реакции и химические формулы
При окислении этилового спирта, обычно присутствующего в процессе производства уксуса, происходит ряд биохимических реакций, в результате которых этиловый спирт окисляется до уксусной кислоты. Процесс окисления можно представить следующими реакциями:
- CH3-CH2-OH → (НАД или НАДФ) → CH3-CH=O + 2 H+
- CH3-CH=O + H2O → (НАД*H2 или НАДФ*H2) → CH3-CH-(OH)2
- CH3-CH-(OH)2 + 1/2 O2 → (КоА) → CH3-CO-OH + 2 H+ + 2 e
- 4 H+ + 4 e + O2 → (система цитохромов, хинонов и флавопротеидов) → 2 H2O
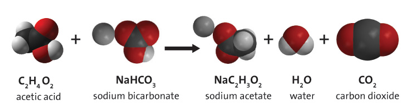
Также интересно отметить, что при реакции между уксусной кислотой и содой образуется ацетат натрия (CH3COONa), растворимый в воде. Реакция выглядит следующим образом:
NaHCO3 + CH3COOH → NaCH3COO + H2O + CO2
В результате реакции образуется углекислый газ (CO2), который выделяется в виде пузырьков, и вода (H2O). Ацетат натрия, полученный в этой реакции, применяется в кулинарии в качестве пищевой добавки и консерванта.
В заключение, уксусная формула (уксусная кислота) обладает свойствами слабой органической кислоты и широко используется в пищевой промышленности, кулинарии и других отраслях.