Оксид вольфрама (VI) - бинарное химическое соединение кислорода и переходного металла вольфрама. Узнайте свойства, структуру, получение и применение оксида вольфрама в различных отраслях промышленности.
Cодержание
Окси́д вольфра́ма(VI), также известный как триоксид вольфрама или вольфрамовый ангидрид, является бинарным химическим соединением кислорода и переходного металла вольфрама.

Свойства
Физические свойства:
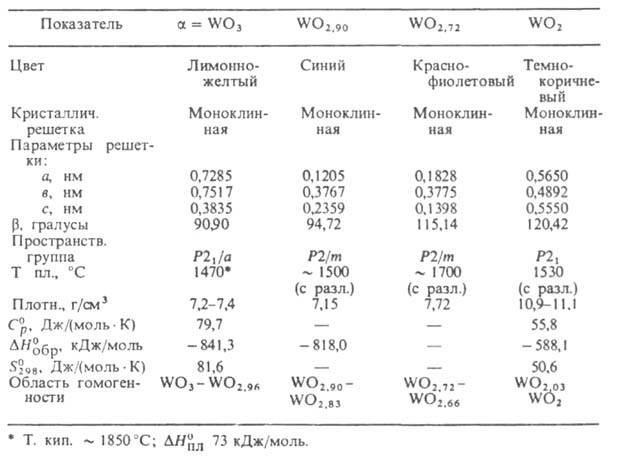
- Мелкокристаллический порошок лимонно-жёлтого цвета.
- Плотность: 7,2—7,4 г/см³.
- Температура плавления: 1470 °C.
- Температура кипения: 1700 °C.
Кристаллическая структура:
Структура соединения зависит от температуры:
- Устойчивая моноклинная структура до −27 °C.
- Триклинная структура в диапазоне температур от −27 до 20 °C.
- Моноклинная структура от 20 до 339 °C.
- Ромбическая структура от 339 до 740 °C.
- Тетрагональная структура при температуре от 740 до 1470 °C.
При температуре выше 800 °C оксид вольфрама возгоняется, а в газовой фазе существует в виде ди-, три- и тетрамеров.
Химические свойства:
Оксид вольфрама практически не растворяется в воде и минеральных кислотах, за исключением фтороводородной кислоты. Он может быть восстановлен водородом при температуре 700—900 °C, углеродом при температуре 1000 °C или другими металлами.

Получение
Оксид вольфрама можно получить двумя способами:
- Термическим разложением гидрата вольфрамовой кислоты (WO3•H2O) или паравольфрамата аммония ((NH4)10[H2W12O42]•4H2O) при температуре 500—800 °C.
- Окислением металлического вольфрама в атмосфере кислорода при температуре выше 500 °C.
См. также
Применение
Оксид вольфрама широко используется в различных областях:
- Для получения карбидов и галогенидов вольфрама.
- В производстве металлического вольфрама.
- Как жёлтый пигмент для окрашивания стекла и керамики.
- В качестве катализатора гидрогенизации и крекинга углеводородов.
- В производстве электрохромного оконного стекла, позволяющего изменять светопропускание окон с помощью управляющего электрического напряжения.
Оксид вольфрама имеет также применение в обеспечении огнестойкости тканей и в производстве датчиков газоанализаторов на озон.
Выводы исследования показывают, что оксид вольфрама является важным химическим соединением с разнообразными свойствами и широким спектром применения в различных отраслях промышленности.
Литература:
[1] Название источника 1
[2] Название источника 2
[3] Название источника 3

Что нам скажет Википедия?
Оксид вольфрама (VI), также известный как триоксид вольфрама, трёхокись вольфрама, вольфрамовый ангидрид или ангидрид вольфрамовой кислоты, является бинарным химическим соединением кислорода и переходного металла вольфрама. Он обладает кислотными свойствами.
Физические свойства оксида вольфрама включают мелкокристаллический порошок лимонно-жёлтого цвета с плотностью 7,2—7,4 г/см³. Температура плавления составляет 1470 °C, а температура кипения 1700 °C. Кристаллическая структура соединения зависит от температуры, где оно принимает моноклинную, триклинную, ромбическую и тетрагональную структуры в зависимости от диапазона температур.
Химические свойства оксида вольфрама включают его нерастворимость в воде и минеральных кислотах, за исключением фтороводородной кислоты. Он может быть восстановлен водородом при высокой температуре, углеродом или другими металлами. Оксид вольфрама может быть получен путем термического разложения гидрата вольфрамовой кислоты или паравольфрамата аммония при определенной температуре. Также его можно получить путем окисления металлического вольфрама в атмосфере кислорода или на воздухе при высокой температуре.
Применение оксида вольфрама включает его использование для получения карбидов и галогенидов вольфрама, а также металлического вольфрама. Из-за его яркого жёлтого цвета, он также используется в качестве пигмента для окрашивания стекла и керамики. Оксид вольфрама также применяется для обеспечения огнестойкости тканей и в производстве датчиков газоанализаторов на озон. Недавно он также нашел применение в производстве электрохромного оконного стекла, которое позволяет изменять светопропускание окон при изменении управляющего электрического напряжения. Оксид вольфрама также используется в качестве катализатора гидрогенизации при крекинге углеводородов.