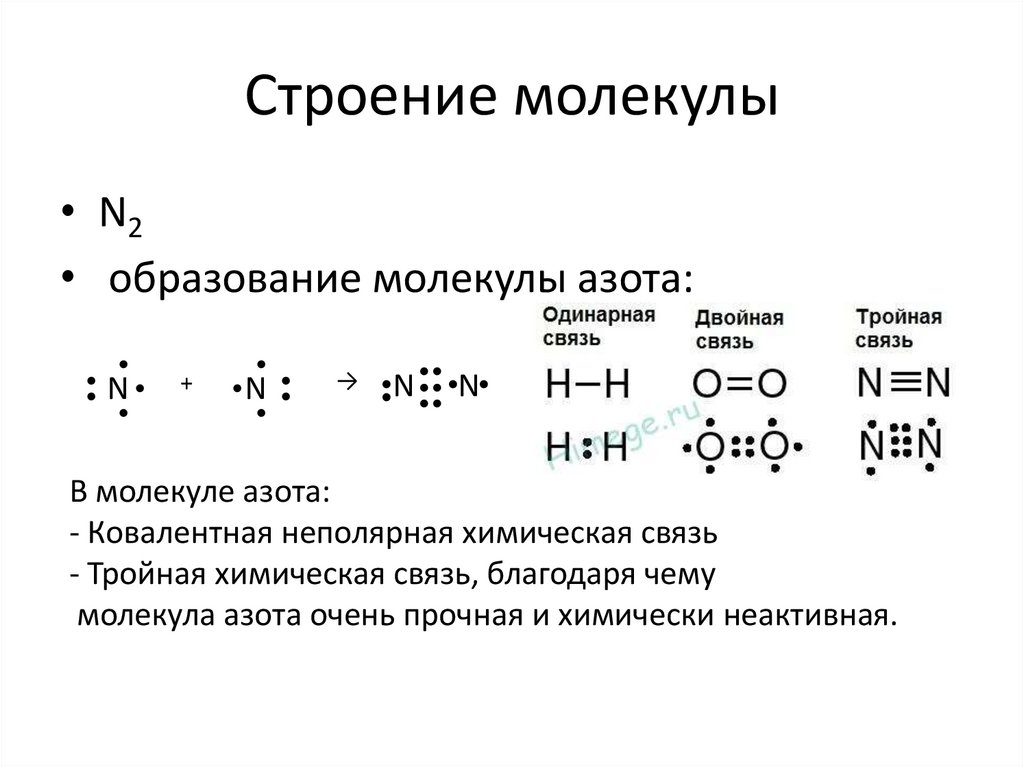
Молекула азота состоит из двух атомов, связанных тройной связью. Узнайте о его электронном строении, физических и химических свойствах, а также о его применении в промышленности и биологии. Также рассмотрим полимерный азот и его особенности.
Cодержание
Электронное строение азота
Атомный номер азота равен 7, что соответствует количеству электронов и протонов в ядре. Молярная масса азота составляет 14,00728 г/моль, а количество нейтронов в атоме равно семи.
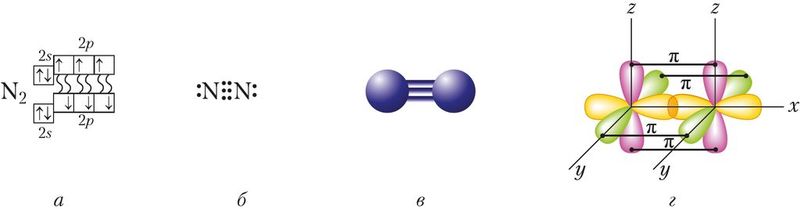
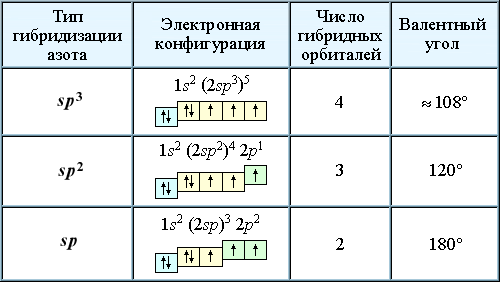
Электронная конфигурация азота в основном состоянии: 1s2 2s2 2p3, а в сокращенном виде — [He]2s2 2p3. На внешнем энергетическом уровне азот имеет 5 валентных электронов, включая 3 неспаренных p-электрона.
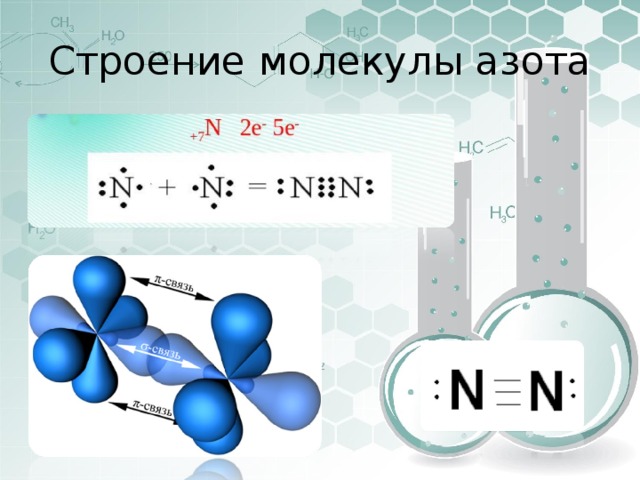
Строение молекулы азота
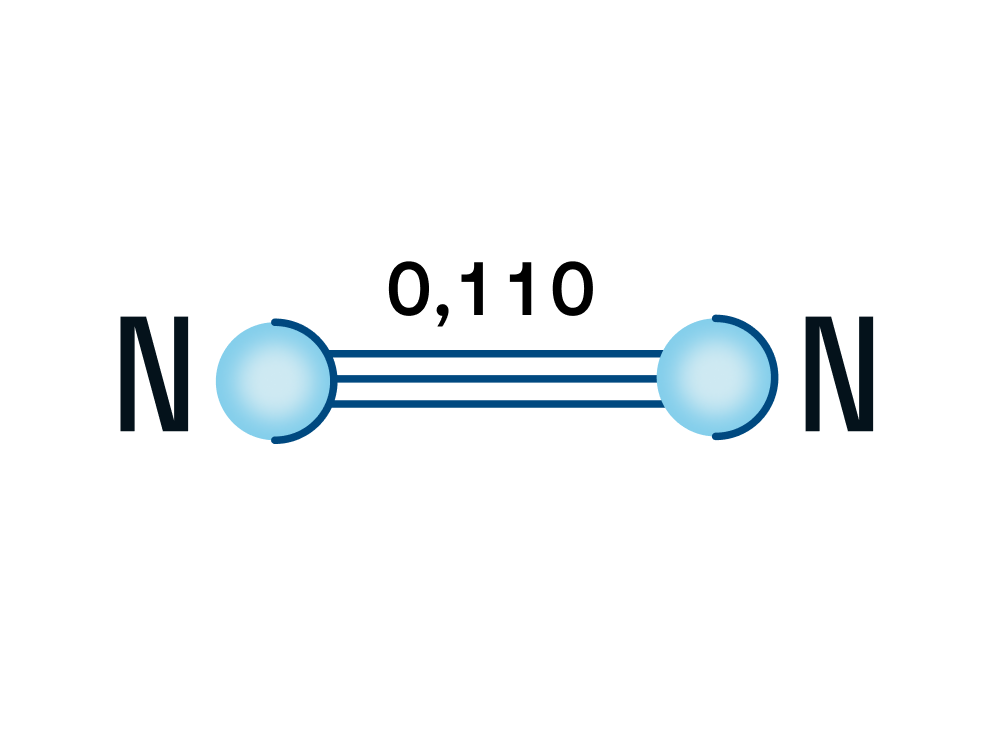
Молекула азота является двухатомной и состоит из атомов, связанных между собой тройной связью. Длина связи между атомами составляет примерно 0,110 нм.
Каждый атом азота имеет 3 неспаренных электрона, которые образуют тройную связь. Такая связь состоит из одной сигма-связи и двух пи-связей.

Физические свойства азота
Азот является бесцветным газом, без запаха и плохо растворимым в воде. Он легче воздуха по своей молярной массе. Из-за прочной тройной связи и небольшого размера атомов азота, у него низкие температуры кипения и плавления: tпл = -210 °С и tкип = -196 °С.
См. также
Химические свойства азота
Атомы азота соединены тройной связью (N≡N), что делает их связь очень прочной. Азот обладает широким спектром возможных степеней окисления от -3 до +5.
Азот химически малоактивный элемент, так как его молекулы разлагаются лишь в незначительной степени даже при высоких температурах. Он может образовывать соединения с другими элементами, особенно с металлами и неметаллами, которые называются нитридами.

Применение азота
Азот широко применяется в промышленности. Жидкий азот используется для охлаждения, замораживания и окисления двигателей ракет. Оксид азота применяется в качестве наркоза и для производства аэрозолей.
Азот также входит в состав аминокислот и нуклеотидов, играя важную роль в биологических процессах.

Полимерный азот
Помимо обычного двухатомного газообразного азота, существует также полимерный азот. В полимерном азоте все атомы связаны одинарными ковалентными связями в трехмерную сетку сложной структуры.
Полимерный азот обладает уникальными свойствами, такими как высокая плотность запасенной химической энергии и сверхтвердость. Он может быть использован в качестве мощного топлива или химической взрывчатки.
Синтез полимерного азота возможен при экстремально высоких давлениях и температурах. Для этого требуются условия, которые могут быть созданы, например, в камерах высокого давления с алмазными наковальнями.
См. также
Заключение
Молекула азота имеет двухатомную структуру, где атомы связаны тройной связью. Азот обладает уникальными физическими и химическими свойствами, что позволяет ему находить применение в различных областях промышленности и биологии. Существует также полимерный азот, который обладает особыми свойствами и может быть использован в качестве мощного топлива или взрывчатки.

Что нам скажет Википедия?
Азот (химический символ — N, от лат. Nitrogenium) — химический элемент 15-й группы (по устаревшей классификации — главной подгруппы пятой группы, VA), второго периода периодической системы Д. И. Менделеева, с атомным номером 7.
Как простое вещество (при н. у.) азот — двухатомный газ (химическая формула — N2) без цвета, вкуса и запаха.
Азот — один из основных биогенных элементов, входящих в состав белков и нуклеиновых кислот.