Степень окисления (окислительное число) — вспомогательная условная величина, используемая для записи процессов окисления, восстановления и окислительно-восстановительных реакций. Она указывает на состояние окисления отдельного атома в молекуле и представляет собой удобный метод учета переноса электронов. Узнайте, как рассчитать и представить степень окисления элементов. Читайте на NOCFN.
Cодержание
Степень окисления (окислительное число) — вспомогательная условная величина, используемая для записи процессов окисления, восстановления и окислительно-восстановительных реакций. Она указывает на состояние окисления отдельного атома в молекуле и представляет собой удобный метод учета переноса электронов.

Определение степени окисления
Степень окисления атома равна численной величине электрического заряда, приписываемого атому в предположении, что электронные пары, осуществляющие связь, полностью смещены в сторону более электроотрицательных атомов. В случае ковалентной связи между одинаковыми атомами электроны делятся поровну между атомами.
Степень окисления соответствует числу электронов, которое следует присоединить к положительному иону, чтобы восстановить его до нейтрального атома, или отнять от отрицательного иона, чтобы окислить его до нейтрального атома.

Представление степени окисления
В научной литературе для обозначения степени окисления элемента используется метод Штока. Степень окисления указывается после названия либо символа элемента римскими цифрами в круглых скобках, без пробела перед открывающей скобкой, например: железо(III), Ni(II).
Степень окисления также может указываться арабскими цифрами сверху над символом элемента.
См. также
Как рассчитать степень окисления
Степень окисления элемента можно рассчитать, учитывая его электроотрицательность. Электроотрицательность можно найти в таблице Менделеева или шкале относительной электроотрицательности. Сравнивая электроотрицательности элементов в соединении, можно определить, кто притягивает электроны и приобретает отрицательный заряд, а кто отдает электроны и получает положительный заряд.
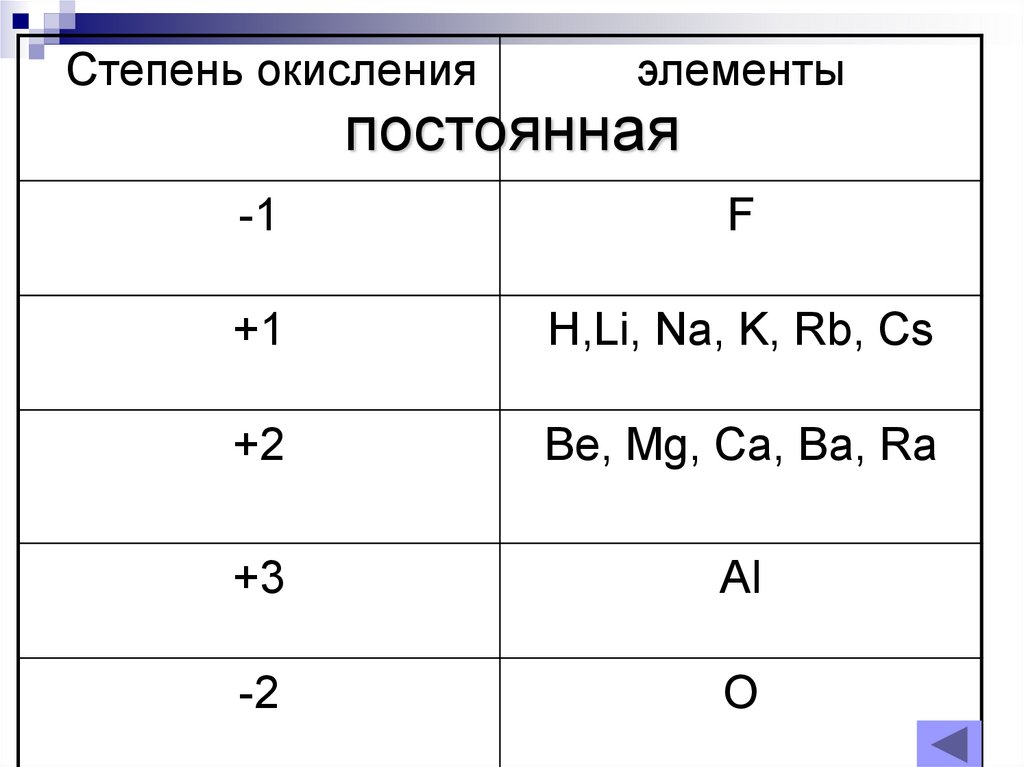
Есть также элементы, которые во всех соединениях отдают или принимают одинаковое количество электронов, и их окислительное число является постоянной величиной.

Примеры расчета степени окисления
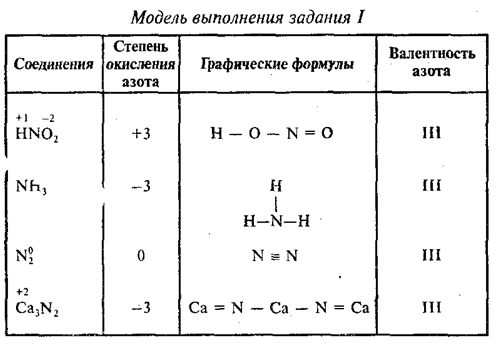
Для наглядности рассмотрим несколько примеров расчета степени окисления.
1. Вещества в химически несвязанном состоянии имеют степень окисления, равную 0. Например, степень окисления Cl2 и S8 равна 0.
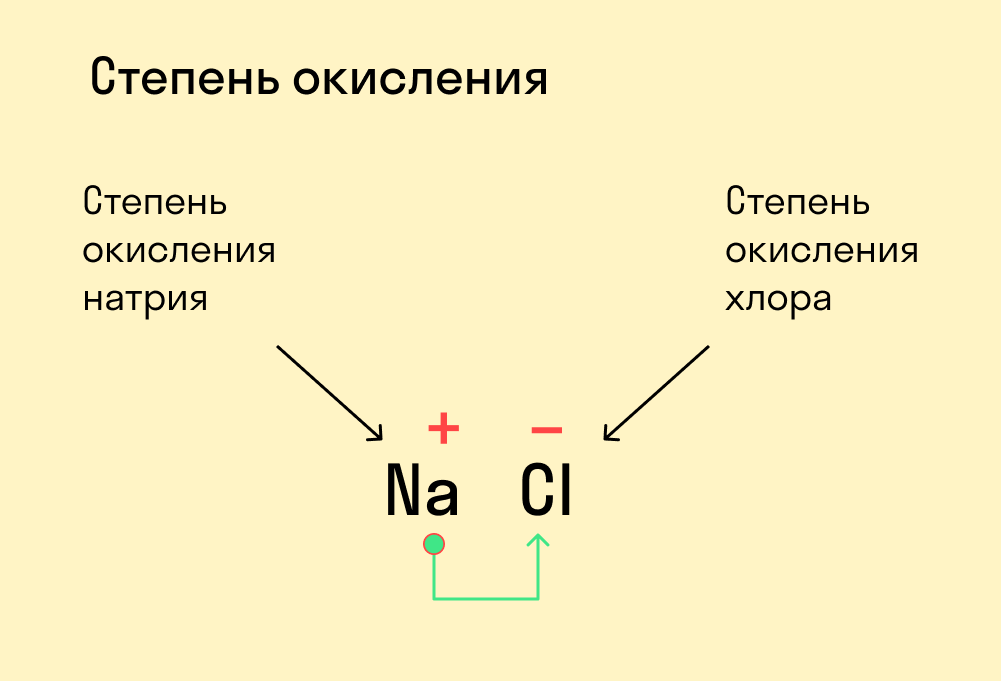
2. В случае соединений, сумма всех степеней окисления в многоатомном ионе равна его заряду. Например, для иона Na+ сумма степеней окисления элементов равна 1, а для иона Cl- сумма степеней окисления элементов равна -1.
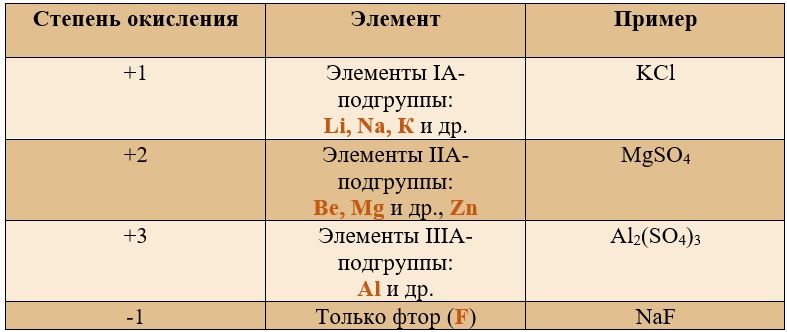
3. Если в соединении есть элементы с известной постоянной степенью окисления, можно использовать эту информацию для расчета степени окисления других элементов. Например, Mg+2 в любом соединении всегда имеет степень окисления +2.
Расчет степени окисления элементов является важным инструментом для классификации химических веществ, описания их свойств, составления формул соединений и их номенклатуры. Он также широко применяется при изучении окислительно-восстановительных реакций.
Итак, степень окисления элементов играет важную роль в химии, позволяя систематизировать и описывать химические соединения. Расчет степени окисления основывается на электроотрицательности элементов и их способности притягивать или отдавать электроны. Использование правил и закономерностей позволяет определить степень окисления элемента в соединении и составить соответствующие формулы и номенклатуру.
Что нам скажет Википедия?
Этот список показывает все известные степени окисления химических элементов. Исключениями являются дробные значения. Наиболее часто встречающиеся степени окисления выделены жирным шрифтом. Этот список основан на таблице Гринвуда со всеми дополнениями. В колонку, в которой степень окисления равна нулю, вписаны инертные газы. Данная таблица базируется на данных Д. И. Менделеева.
Аналогичный график был использован Ирвингом Ленгмюром в 1919 году в своих самых ранних стадиях изучения правила октета.