Узнайте, какая химическая связь образуется между атомами азота и водорода. Разберем механизм образования ковалентной связи и ее влияние на свойства молекулы. Изучите примеры образования молекулы хлороводорода и воды.
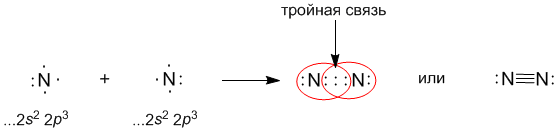
На примере ковалентных связей удобно описывать механизм химической связи в целом. Впервые это сделал американский ученый Гилберт Льюис, анализируя взаимодействие между частицами в молекулах водорода, азота, кислорода и других простых неметаллов.
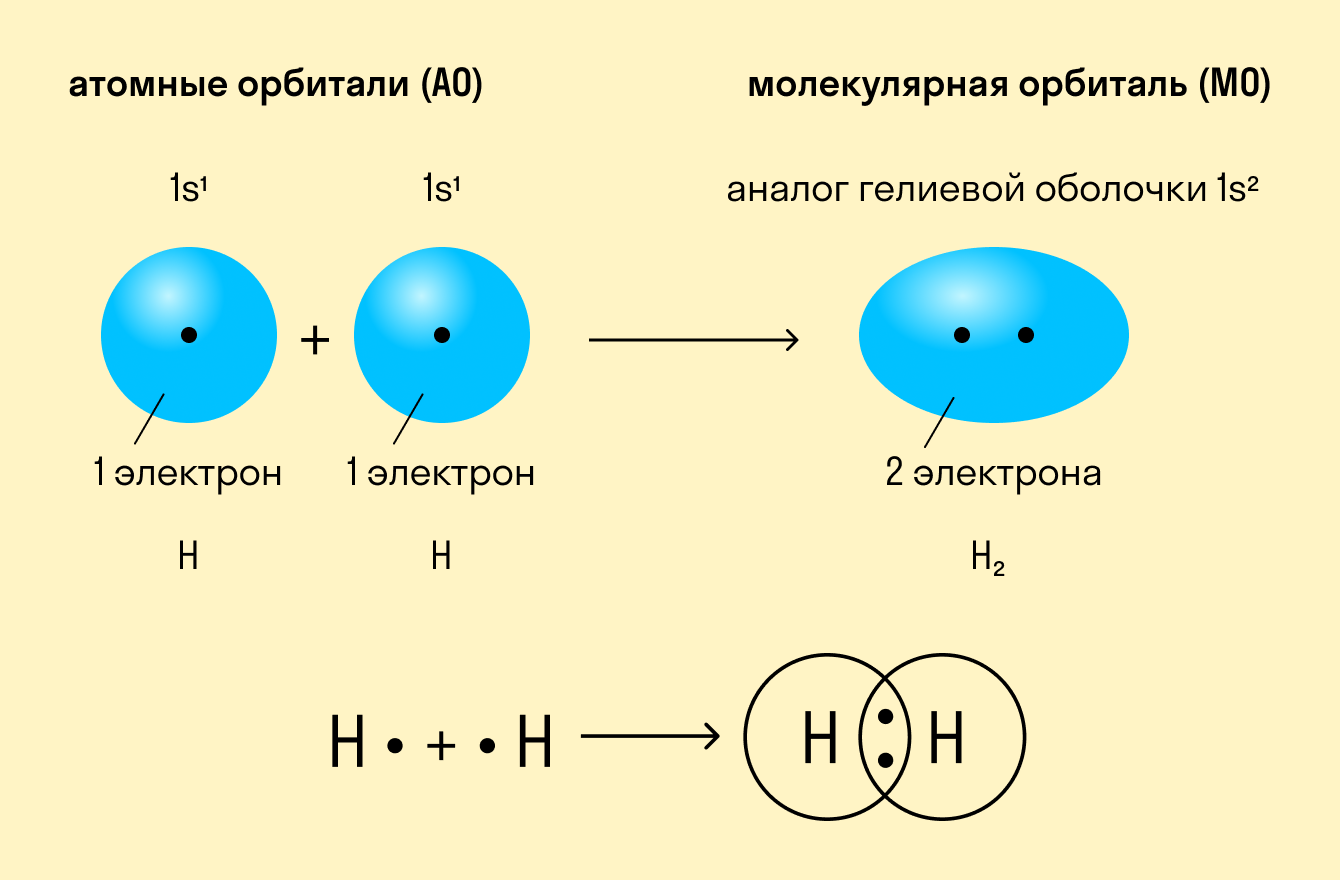
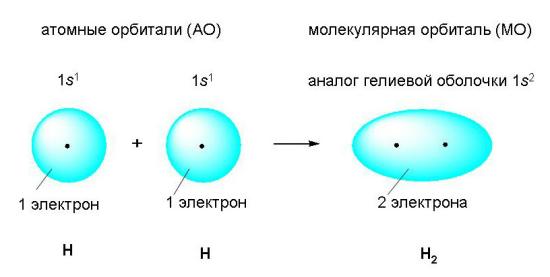
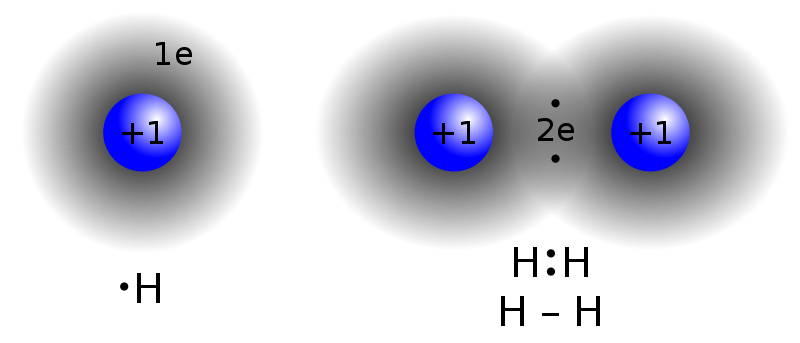
Как происходит такое взаимодействие? Атом водорода отличается очень простым строением — его электронное облако или орбиталь содержит лишь один свободный (валентный) электрон. При сближении двух атомов водорода их орбитали пересекаются и начинают частично перекрывать друг друга.
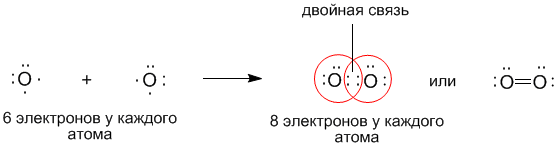
Свободные электроны на этих орбиталях объединяются в пару, которая принадлежит обоим участникам взаимодействия. Это и есть процесс образования ковалентной связи. По ее итогам каждый атом имеет уже два электрона и приобретает устойчивую внешнюю оболочку. Общие электронные пары, образующиеся в простых веществах H2, O2, Cl2, F2, N2, в одинаковой степени принадлежат обоим атомам. Такая ковалентная связь называется неполярной.
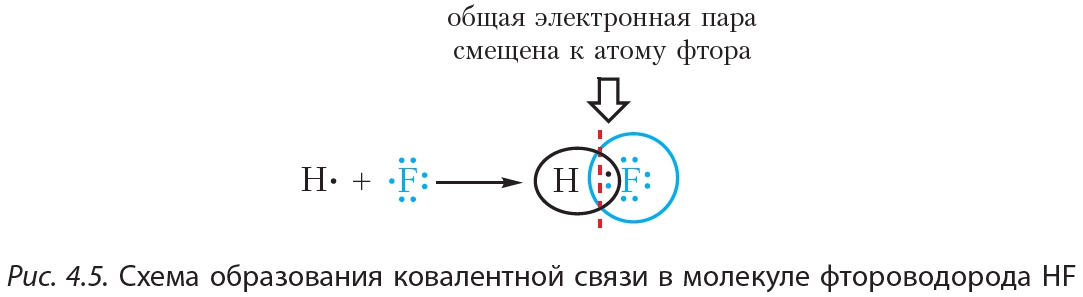
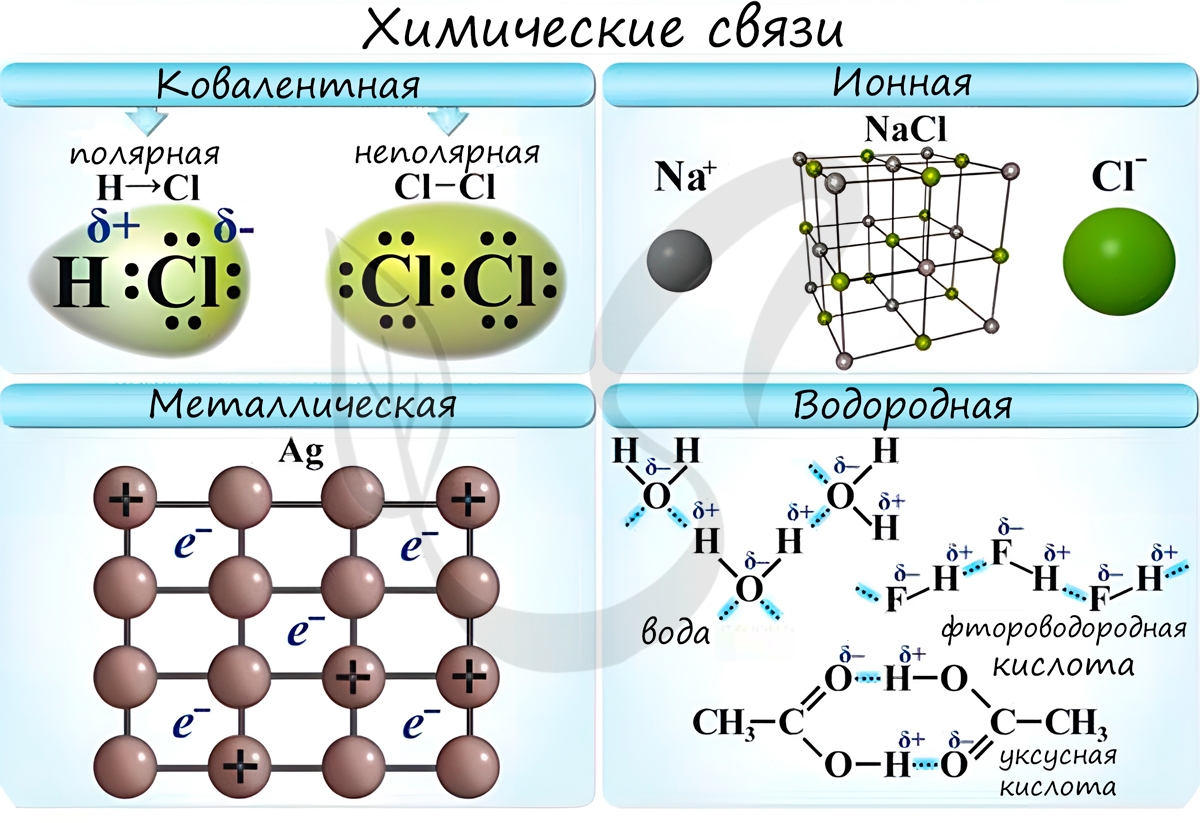
Если ковалентная связь образуется между разными атомами, то общая электронная пара смещается к тому из них, который имеет более высокую электроотрицательность (ЭО). Он получает частичный отрицательный заряд. Атом, имеющий меньшую ЭО, становится заряжённым положительно. В этом случае образуется полярная ковалентная связь.
Образование молекулы хлороводорода
У атома водорода на внешнем уровне — один электрон. У хлора на внешнем уровне — семь электронов, один из которых неспаренный.
Образуется одна общая электронная пара, которая смещена к атому хлора. В результате появляются частичные заряды: на атоме хлора — отрицательный, а на атоме водорода — положительный. Сдвиг электронной плотности принято обозначать греческой буквой дельта δ.
Рис. 1. Образование молекулы хлороводорода
| Структурная формула | Химическое обозначение |
|---|---|
| H−Cl | хлороводород |

Образование молекулы воды
На внешнем уровне атома кислорода — шесть электронов, два из которых неспаренные.
Атом кислорода образует две общие электронные пары с двумя атомами водорода.
Электронная плотность этих общих пар сдвинута к более электроотрицательному кислороду. Атом кислорода имеет отрицательный заряд, а атомы водорода — положительный.
Рис. 2. Образование молекулы воды
| Структурная формула | Химическое обозначение |
|---|---|
| H−O−H | вода |
Таким образом, между атомами азота и водорода образуется ковалентная связь, которая может быть неполярной или полярной в зависимости от электроотрицательности атомов. Это обеспечивает стабильность молекулы и ее химические свойства.
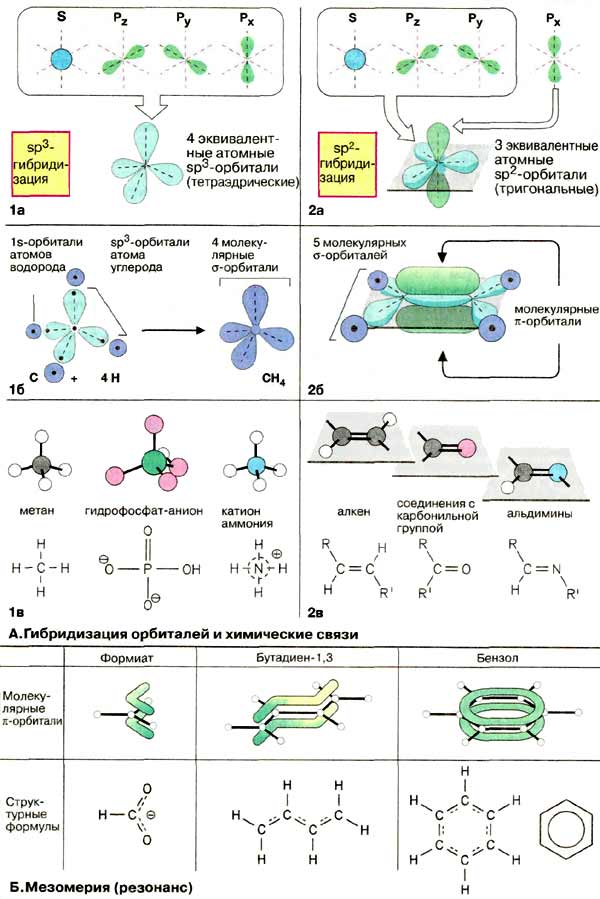
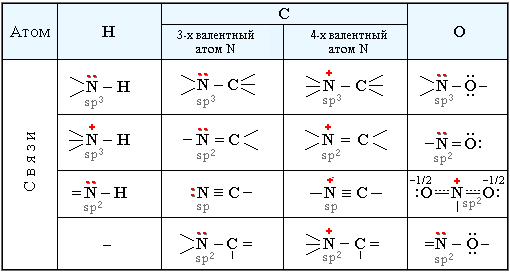
Ковалентная связь является одной из основных форм химической связи и имеет различные типы, такие как σ-связь, π-связь и др. Она определяет направленность, насыщаемость, полярность и поляризуемость молекулы, влияя на ее химические и физические свойства.
Углы между двумя ковалентными связями называются валентными. Ковалентные связи могут быть неполярными, если молекула состоит из одинаковых атомов, или полярными, если молекула состоит из атомов разных химических элементов и имеет асимметрию распределения электрического заряда в молекуле.
В итоге, ковалентная связь между атомами азота и водорода играет ключевую роль в образовании молекулы аммиака (NH3) и определяет ее свойства и реакционную способность.