Производство серной кислоты из воды является процессом получения этой кислоты из исходного сырья в промышленных масштабах. Узнайте о различных методах производства и свойствах серной кислоты.
Cодержание
Производство серной кислоты
Производство серной кислоты является процессом получения этой кислоты из исходного сырья в промышленных масштабах. Несмотря на то, что серная кислота давно известна, первоначально её получали сухой перегонкой - термическим разложением купоросов. В промышленных количествах она стала производиться относительно недавно.
Камерный способ
С середины XIV века серную кислоту получали с помощью так называемого "камерного" метода. Основой этого метода была реакция горения на воздухе смеси серы и калийной селитры. Процесс проводился в свинцовых камерах, нерастворимых в серной кислоте. Результатом горения были оксиды азота, соли калия и SO3. Последний поглощался водой, находящейся в камере. Таким способом удавалось получать кислоту небольшой крепости, которую затем концентрировали известными методами.
В зависимости от соотношения реагентов получался разный состав твердого остатка. Промышленные количества камерной серной кислоты получали во Франции и Англии. В СССР камерный способ использовался до 1955 года. После обнаружения каталитической роли оксидов азота в реакции образования SO3, от камерного способа стали отказываться в пользу менее трудоемких и более эффективных методов, использующих окисление SO2.
Современные способы
В настоящее время для получения серной кислоты используют различные сырьевые материалы. Основными из них являются элементарная сера, сульфиды и сульфаты металлов, сероводород, отходящие газы теплоэлектростанций, использующих неочищенную нефть и другие. Ранее основным сырьем был пирит, но его использование снизилось в последние годы. Например, в 1958 году в СССР из пирита было получено 71,4% серной кислоты производства за этот год, а к 1970 году доля пирита снизилась до 41,8%.
На сегодняшний день основным сырьем для производства серной кислоты является сера. В 2011 году в России из общего количества в 10,7 млн тонн произведенной серной кислоты, 7,9 млн тонн получено из серы, а 2,8 млн тонн - из отходящих газов и нефтепереработки. В мире в 2011 году из общего количества в 223 млн тонн произведенной серной кислоты, 136 млн тонн получено из серы, 67 млн тонн - из отходящих газов и 20 млн тонн - из пирита. Китай является лидером в производстве серной кислоты в мире.

Свойства серной кислоты
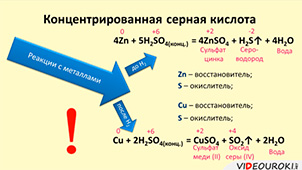
Серная кислота (H2SO4) является сильной неорганической кислотой с высшей степенью окисления серы (+6). При обычных условиях концентрированная серная кислота представляет собой тяжелую маслянистую жидкость без цвета и запаха, с сильно кислым "медным" вкусом. В технике серной кислотой называют как смеси с водой, так и с серным ангидридом SO3. Если молярное отношение SO3 : H2O 1, то это водный раствор серной кислоты, если > 1 - раствор SO3 в серной кислоте (олеум). Серная кислота обладает исключительно сильной коррозионной активностью и является токсичной в больших дозах.

Исторический контекст
Серная кислота была известна с древности и встречается в природе в свободном виде, например, в виде озер вблизи вулканов. Способы получения серной кислоты были описаны алхимиками разных времен и народов. Одним из ранних способов получения серной кислоты было прокаливание смеси железного и медного купороса, что было сделано в IX веке персидским алхимиком Ар-Рази. Алхимик Василий Валентин в XVI веке описал способ получения серной кислоты путем поглощения водой газа, выделяющегося при сжигании смеси порошков серы и селитры. Этот способ впоследствии стал основой "камерного" способа, который использовался в СССР до 1955 года. В настоящее время применяются современные методы получения серной кислоты, которые более эффективны и экономичны.
См. также
Процесс получения серной кислоты
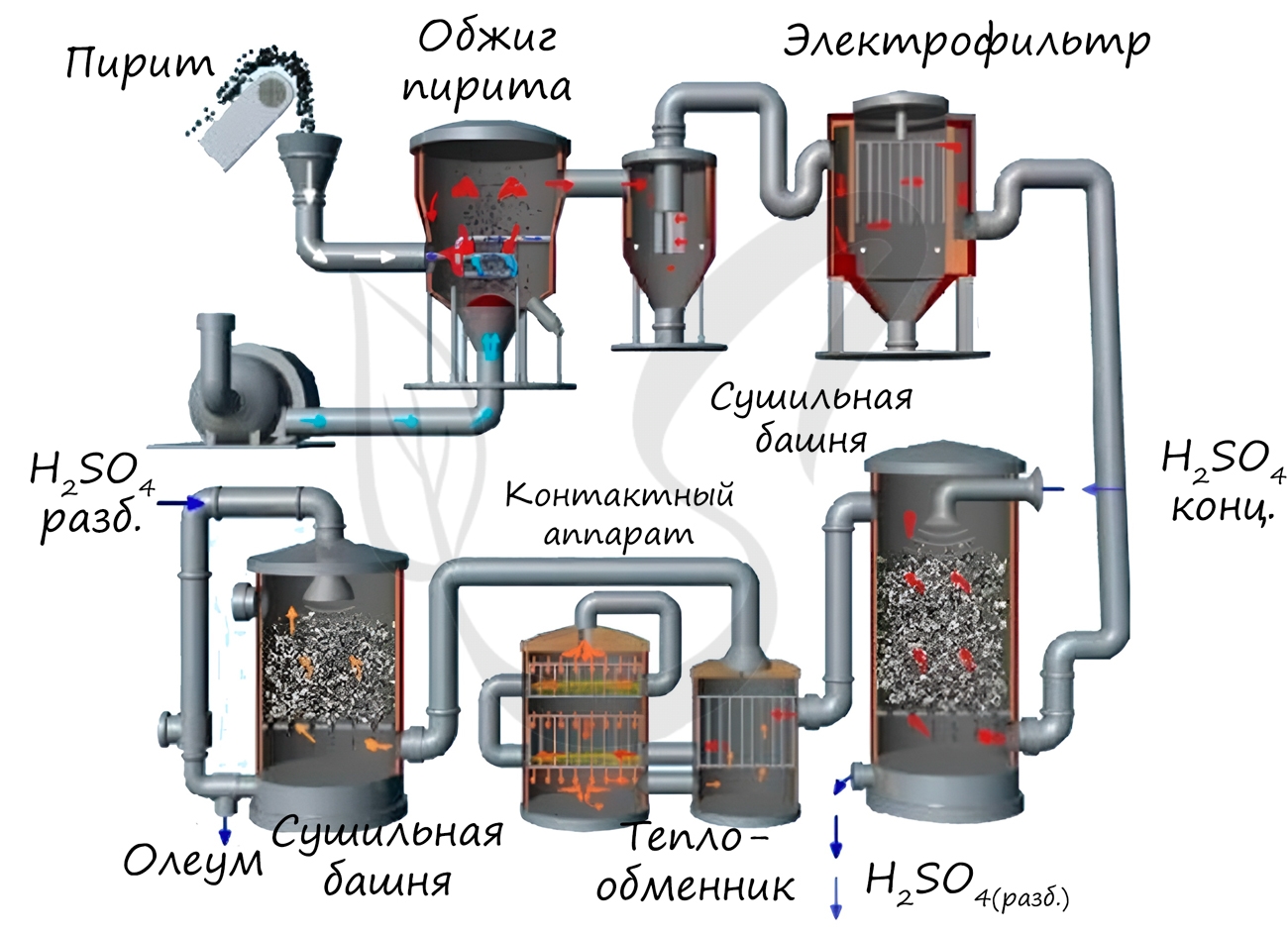
В настоящее время процесс получения серной кислоты осуществляется каталитическим окислением оксида серы (IV) при помощи оксида ванадия (V2O5). Образовавшийся олеум, содержащий различные концентрации серной кислоты и SO3, затем проходит процесс концентрирования и фильтрации. После этого серная кислота готова к использованию и может быть отправлена потребителю.

Что нам скажет Википедия?
Как получить серную кислоту из воды?