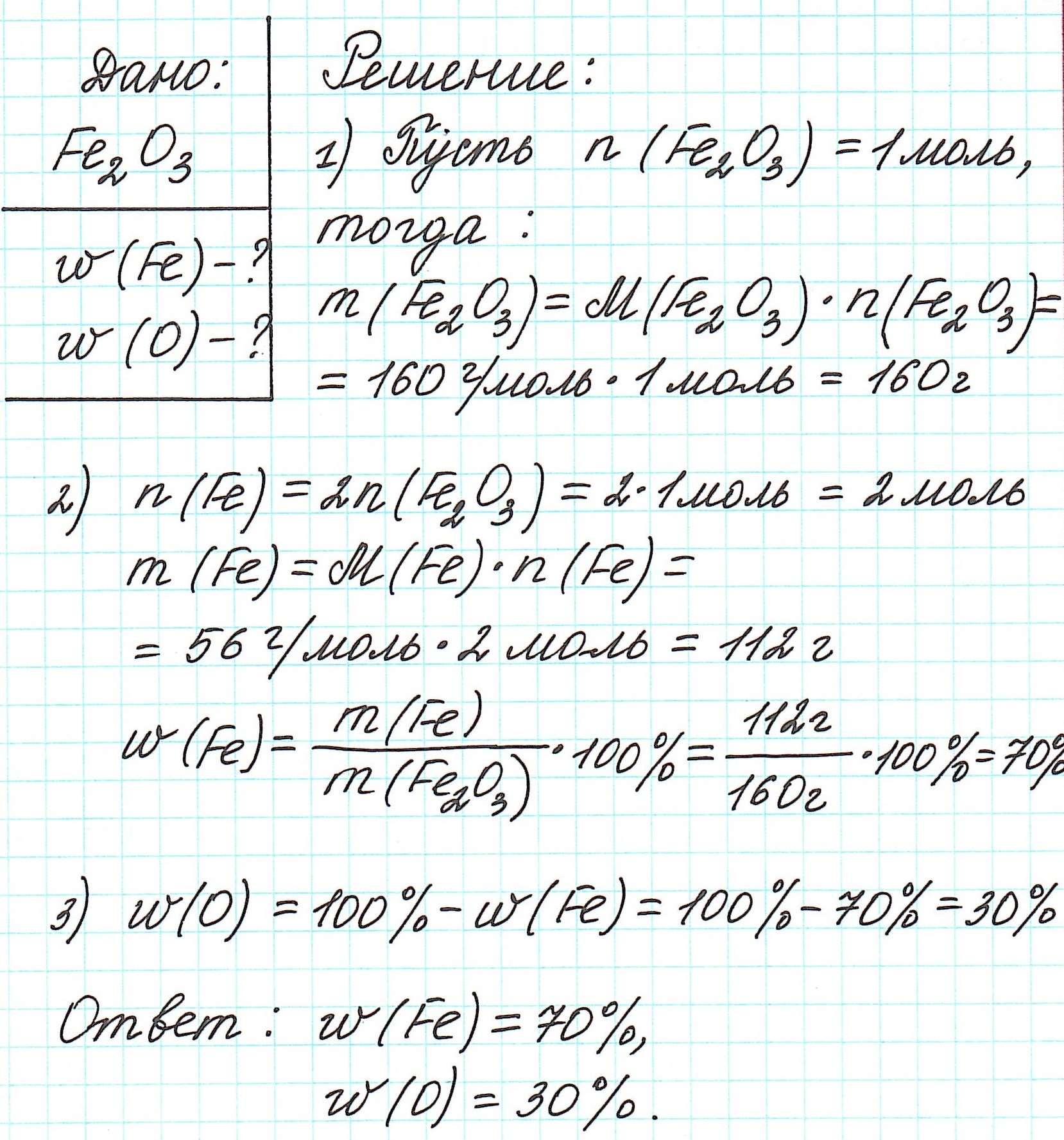Узнайте, как найти количество вещества (n) в химии формулы. Решайте задачи с использованием массы, объема и молярной массы вещества. Упростите вычисления с помощью количества вещества в моль. Научитесь применять закон сохранения массы в химических уравнениях. Используйте молярные объемы газа и числа Авогадро для определения количества вещества. | NOCFN
Cодержание
В химии решение основных задач связано с использованием нескольких важных понятий и формул. Все вещества имеют разную массу, плотность и объем. Кусочек одного металла может весить во много раз больше, чем точно такой же размер кусочка другого металла.

Моль (количество моль)
Моль (обозначение: моль, международное: mol) является единицей измерения количества вещества. Она соответствует количеству вещества, в котором содержится NA частиц (молекул, атомов, ионов). Часто встречающаяся фраза в задачах - "было получено... моль вещества".
NA = 6,02 · 1023
NA - число Авогадро, которое равно количеству частиц (атомов, молекул, ионов) в 1 моле вещества. Для удобства оперирования такими величинами химики и физики всего мира договорились обозначать 6,02 · 1023 частиц как 1 моль вещества.
1 моль = 6,02 · 1023 частиц

Молярная масса вещества
Молярная масса вещества - это масса одного моля вещества. Она обозначается как M.
Также существует понятие молекулярной массы - Mr, которая определяется как сумма атомных масс вещества. Например, для серной кислоты (H2SO4) молярная масса будет равна 98 г/моль.
См. также
Формула массы вещества
Для нахождения массы вещества нам необходимо знать количество моль (n), которое можно получить из Периодической системы.
Также следует учитывать закон сохранения массы - масса веществ, вступивших в химическую реакцию, всегда равна массе образовавшихся веществ.

Формула объема вещества
Объем вещества может быть найден на основании закона Авогадро, согласно которому в равных объемах различных газов, взятых при одинаковых температуре и давлении, содержится одно и то же число молекул.
Таким образом, в химии количество вещества используется для измерения макроскопических количеств веществ во многих естественных науках, таких как физика, химия, электролиз, термодинамика. При описании химических реакций удобнее использовать количество вещества, чем массу.
Определение, единицы измерения, обозначение
Количество вещества измеряется в молях (моль) по международной системе единиц (СИ). В химии это количество однотипных структурных единиц, таких как атомов, электронов, молекул, ионов и других частиц, и обозначается как n.
См. также
Применение и значение
В химии при написании химических уравнений количество вещества играет важную роль после знакомства со законом сохранения массы вещества. Например, при реакции горения водорода требуется 2 к 1 количеству кислорода. Зная массу водорода, можно получить количество вещества кислорода, участвующего в реакции.
В реальных опытах вместо количества вещества "в штуках" использование молярной массы (г/моль) упрощает вычисления и сокращает соотношение исходных реактивов. В 1 моле содержится 6 · 1023 частиц, что называется числом Авогадро (NA).
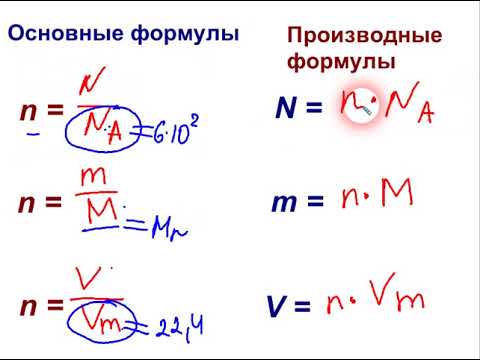
Для вычисления количества вещества на основе его массы используется молярная масса, которая вычисляется как отношение массы вещества к количеству молей:
n = m/M,
где m - масса вещества, M - молярная масса вещества.
Также молярная масса может быть найдена как произведение молекулярной массы вещества на количество молекул в 1 моле (число Авогадро).
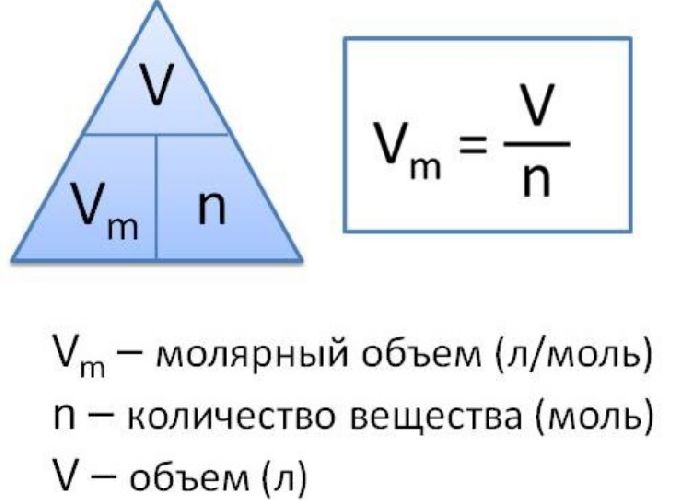
Количество вещества газообразного вещества определяется на основе его объема:
n = V / Vm,
где V - объем газа при нормальных условиях, Vm - молярный объем газа при тех же условиях, равный 22,4 л/моль по закону Авогадро.
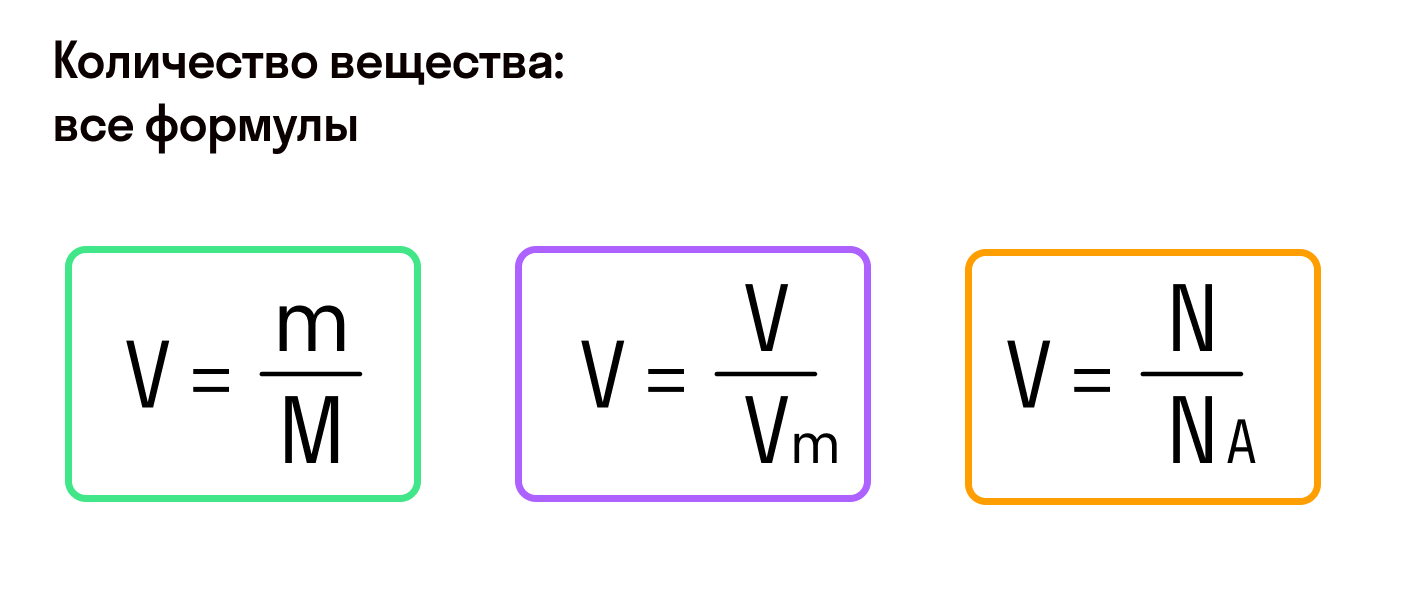
Итак, для решения задач по химии с использованием количества вещества можно использовать общую формулу:
n = m/M или n = V / Vm,
где n - количество вещества, m - масса вещества, M - молярная масса вещества, V - объем газа, Vm - молярный объем газа.
Вычисления
Давайте решим простую задачу для более полного понимания использования количества вещества. Пусть у нас есть алюминиевая отливка массой m = 5,4 кг. Чтобы найти количество вещества в данной отливке, мы можем использовать формулу:
n = m/M,
где m - масса вещества, M - молярная масса вещества. По таблице Менделеева мы можем найти молярную массу алюминия (Al) и использовать ее в формуле, чтобы получить количество вещества в отливке.
Таким образом, мы можем использовать количества вещества в химии для решения различных задач, таких как расчет массы, объема или количества реагентов в химических реакциях.