Открытие атома является одним из самых значимых событий в истории науки и технологий. Узнайте, что содержит атом и какие свойства у него есть. Познакомьтесь с ролью атома в различных областях, таких как ядерная энергетика, медицина и химическая промышленность. Исследуйте перспективы исследования атома в современной науке.
Открытие атома
Открытие атома является одним из самых значимых событий в истории науки и технологий. Атом был открыт в середине XIX века благодаря работам таких ученых, как Антуан де Бройль, Эрнест Резерфорд, Нильс Бор и другие.
Первым открывателем атома был древнегреческий философ Демокрит. В своей работе "О природе" он утверждал, что атомы являются причиной всех явлений в мире. Ученый также утверждал, что материя состоит из атомов, которые могут объединяться или разделяться, образуя различные комбинации.
В 1869 году английский физик Джеймс Клерк Максвелл опубликовал свою теорию электромагнитных волн, которая описывала свет как поток частиц - фотонов. Это открытие стало первым шагом к пониманию того, что свет состоит из отдельных частиц, а не является непрерывной волной.
Однако, чтобы доказать существование атомов, потребовалось еще несколько десятилетий исследований и экспериментов. В 1909 году Эрнест Резерфорд и его коллеги провели эксперимент, который показал, что атомы состоят из более мелких частиц - протонов и нейтронов, и что они имеют положительный заряд.
Только в 1911 году Нильс Бор предложил свою модель атома, которая объяснила, как электроны могут вращаться вокруг ядра и как они могут испускать и поглощать свет. Эта модель стала основой для понимания структуры атома и его свойств.
Открытие атома стало одним из ключевых моментов в развитии науки и технологии. Оно позволило понять природу материи и света, а также создать новые материалы и технологии, которые используются сегодня во многих отраслях промышленности.
Характеристики атома
Масса атома
Масса атома (или атомная масса) - это физическая величина, характеризующая инертные свойства атома. Она определяет, насколько сильно атом сопротивляется изменению своей скорости или направления движения.
Атомная масса измеряется в единицах атомной массы, называемых а.е.м. (атомные единицы массы). Одна а.е.м. равна 1/12 массы атома углерода-12 (C).
Обычно атомная масса выражается целым числом, которое соответствует массе самого легкого атома данного элемента. Например, атомная масса углерода равна 12, а атома кислорода - 16.
Строение атома
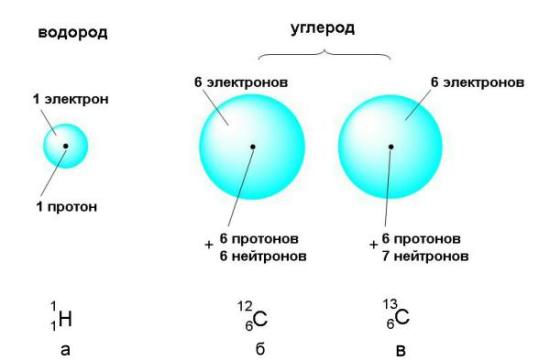
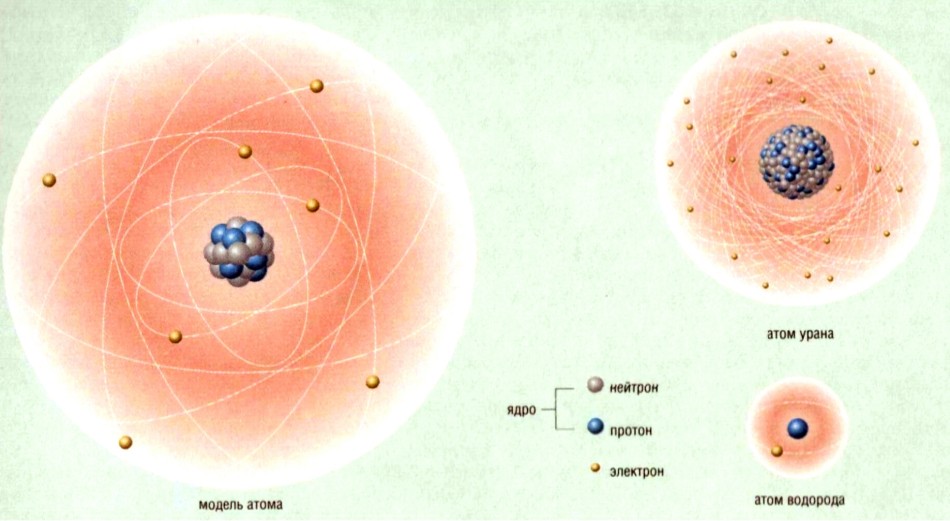
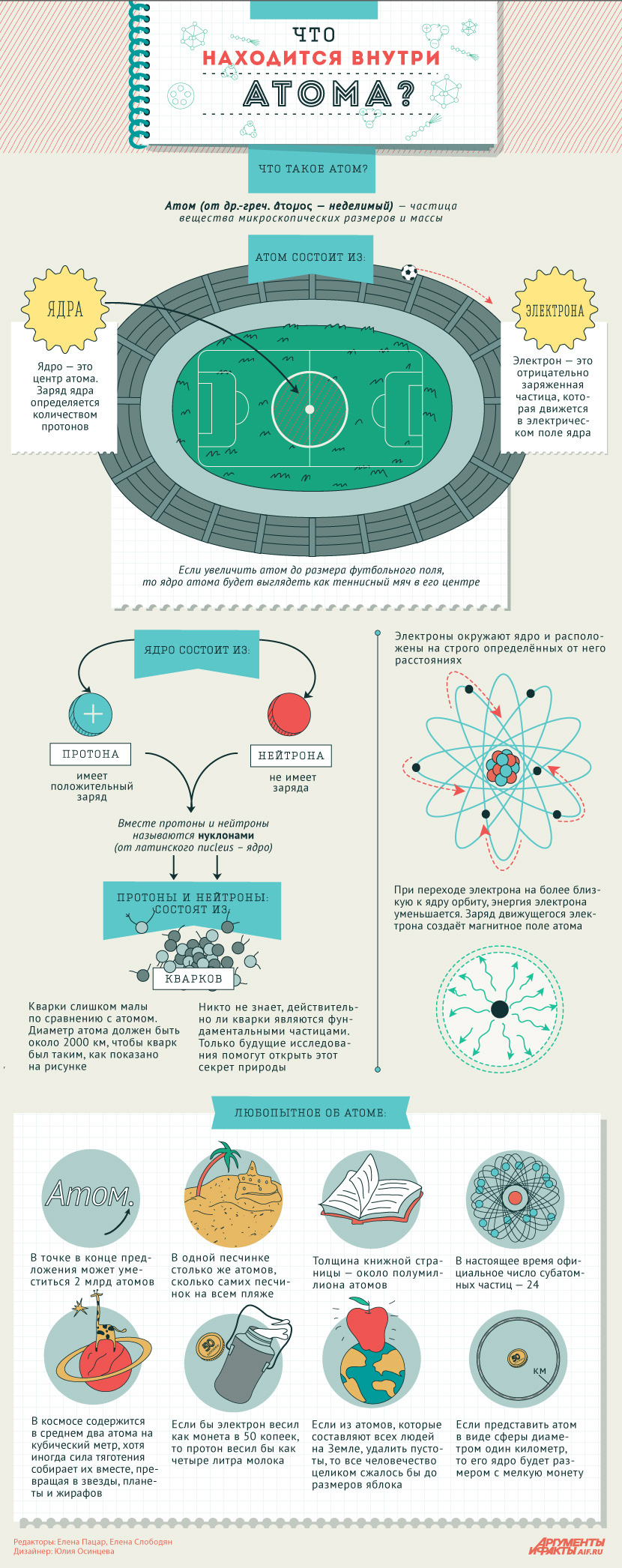
Атом — это наименьшая частица химического элемента, сохраняющая все его химические свойства. Атом состоит из ядра и вращающихся вокруг него электронов. Ядро также имеет сложное строение и состоит из нейтронов и протонов.
Число электронов равно числу протонов в атоме и определяется порядковым номером. В связи с этим атом в целом электронейтрален, так как электроны заряжены отрицательно, а протоны положительно. Заряд ядра также равен порядковому номеру. Число нейтронов рассчитывается по формуле N = A - Z, где N — общее число нейтронов, А — массовое число, Z — заряд ядра.
Число энергетических уровней в атоме определяется номером периода. Число электронов на последнем внешнем уровне равно номеру группы.
Максимальное число электронов на энергетическом уровне определяется формулой N = 2 * n^2, где N — общее число электронов на энергетическом уровне, n - номер уровня.
Каждый энергетический уровень делится на подуровни. На первом уровне только один подуровень — s. На втором уровне два подуровня — s и p. на третьем — s, p и d. На четвертом — s, p, d и f.
Свойства атома
Атомы обладают различными свойствами, которые определяют их поведение в химических реакциях и взаимодействиях с другими атомами.
Одно из основных свойств атома - его электрический заряд. Протоны в ядре атома имеют положительный заряд, а электроны - отрицательный заряд. Это обусловливает электронное строение атома и его взаимодействие с другими атомами.
Важным свойством атома является его размер. Размер атома определяется расстоянием между ядром и электронной оболочкой. Чем больше число электронов в атоме, тем больше его размер.
Другое важное свойство атома - его масса. Масса атома определяется суммой масс протонов и нейтронов в ядре. Масса атома выражается в атомных единицах массы (а.е.м.), где одна а.е.м. равна 1/12 массы атома углерода-12.
Применение атома
Атомы имеют широкий спектр применений в различных областях. Одно из наиболее известных применений атома - ядерная энергетика. Разделение атомов ядерными реакциями позволяет получить большое количество энергии, которая используется в производстве электроэнергии и других отраслях промышленности.
Атомы также используются в медицине для диагностики и лечения различных заболеваний. Различные методы образования изображений, такие как компьютерная томография и ядерная магнитно-резонансная томография, основаны на взаимодействии атомов вещества с электромагнитным излучением.
В химической промышленности атомы используются для создания новых материалов и соединений. Многие химические реакции основаны на перестройке атомов вещества, что позволяет получать различные продукты и соединения.
См. также
Перспективы исследования
Исследование атома и его свойств является одной из основных задач современной науки. С развитием технологий и научных методов становится возможным изучение атомов с все большей точностью и детализацией.
Одной из перспективных областей исследования атома является нанотехнология, которая основана на манипулировании атомами для создания новых материалов и устройств с уникальными свойствами.
Также активно исследуются свойства экзотических атомов, которые содержат необычные частицы или имеют необычную структуру. Эти исследования могут привести к новым открытиям и разработке новых технологий в различных областях науки и промышленности.
Что нам скажет Википедия?
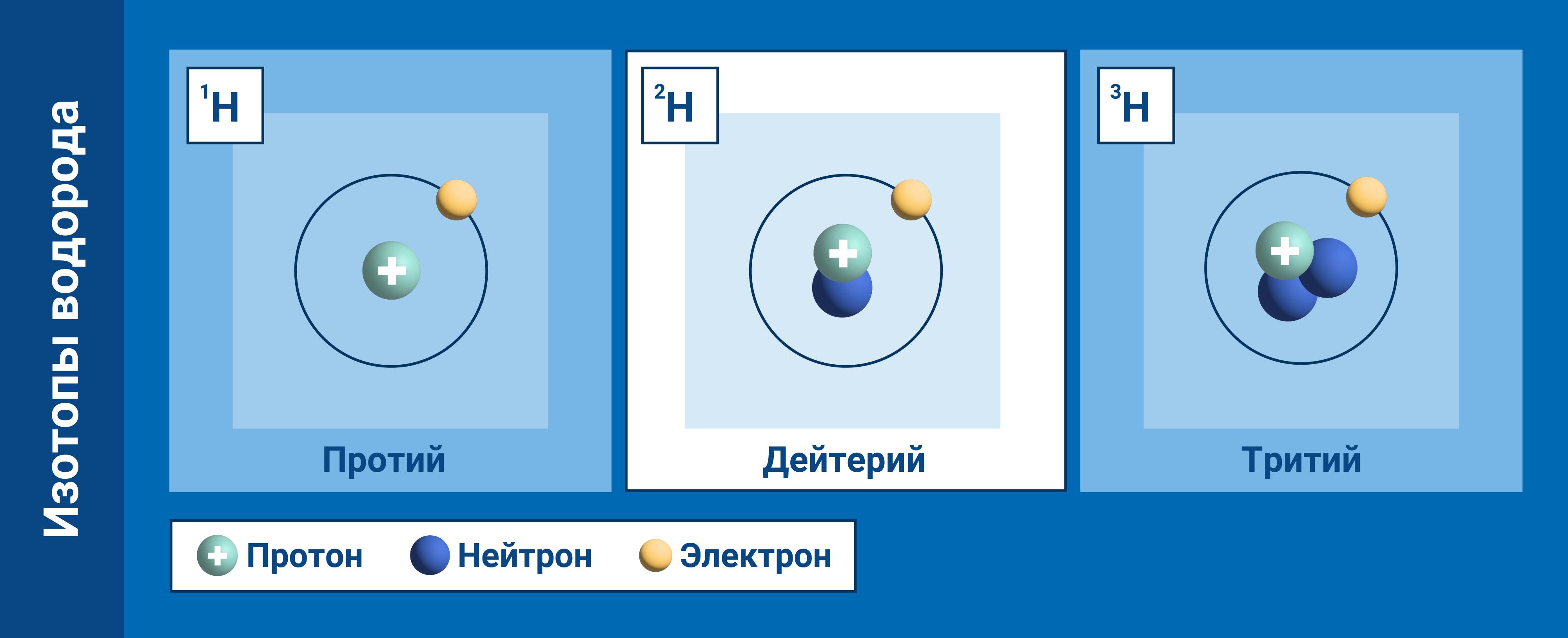
Атомы состоят из ядра и электронов (точнее, электронного «облака»). Ядро атома состоит из протонов и нейтронов. Количество нейтронов в ядре может быть разным: от нуля до нескольких десятков. Если число электронов совпадает с числом протонов в ядре, то атом в целом оказывается электрически нейтральным. В противном случае он обладает некоторым положительным или отрицательным зарядом и называется ионом. В некоторых случаях под атомами понимают только электронейтральные системы, в которых заряд ядра равен суммарному заряду электронов, тем самым противопоставляя их электрически заряженным ионам.
Ядро, несущее почти всю (более чем 99,9 %) массу атома, состоит из положительно заряженных протонов и незаряженных нейтронов, связанных между собой при помощи сильного взаимодействия. Атомы классифицируются по количеству протонов и нейтронов в ядре: число протонов Z соответствует порядковому номеру атома в периодической системе Менделеева и определяет его принадлежность к некоторому химическому элементу, а число нейтронов N — определённому изотопу этого элемента. Единственный стабильный атом, не содержащий нейтронов в ядре — лёгкий водород (протий). Число Z также определяет суммарный положительный электрический заряд (Z×e) атомного ядра и число электронов в нейтральном атоме, задающее его размер.