Атом (от др.-греч. ἄτομος «неделимый, неразрезаемый») — частица вещества микроскопических размеров и массы, наименьшая часть химического элемента, являющаяся носителем его химических свойств. Узнайте больше о структуре и свойствах атомов в этой статье.
Cодержание
Атом (от др.-греч. ἄτομος «неделимый, неразрезаемый») — частица вещества микроскопических размеров и массы, наименьшая часть химического элемента, являющаяся носителем его химических свойств.

Структура атома
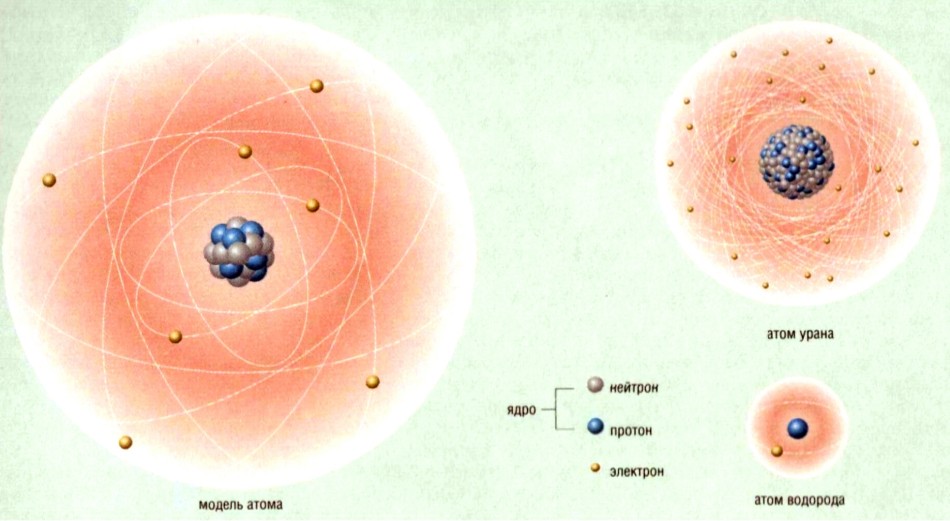
Атомы состоят из ядра и электронов. Ядро атома состоит из протонов и нейтронов. Количество нейтронов в ядре может быть разным: от нуля до нескольких десятков. Если число электронов совпадает с числом протонов в ядре, то атом в целом оказывается электрически нейтральным. В противном случае он обладает некоторым положительным или отрицательным зарядом и называется ионом. В некоторых случаях под атомами понимают только электронейтральные системы, в которых заряд ядра равен суммарному заряду электронов, тем самым противопоставляя их электрически заряженным ионам.
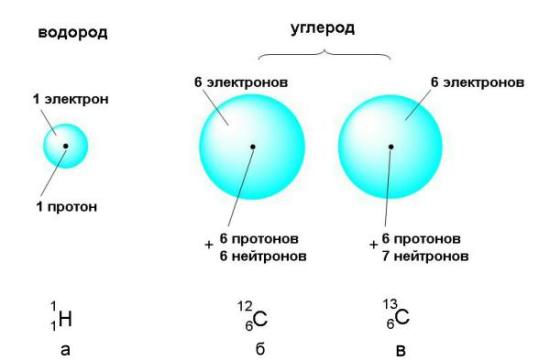
Ядро атома несёт почти всю (более чем 99,9%) массу атома и состоит из положительно заряженных протонов и незаряженных нейтронов, связанных между собой при помощи сильного взаимодействия. Атомы классифицируются по количеству протонов и нейтронов в ядре. Число протонов Z соответствует порядковому номеру атома в периодической системе Менделеева и определяет его принадлежность к некоторому химическому элементу, а число нейтронов N определяет изотоп этого элемента. Единственный стабильный атом, не содержащий нейтронов в ядре, является лёгким водородом (протий). Число Z также определяет суммарный положительный электрический заряд (Z×e) атомного ядра и число электронов в нейтральном атоме, задающее его размер.

История становления понятия
Понятие об атоме как о наименьшей неделимой части материи было впервые сформулировано древнеиндийскими и древнегреческими философами. В XVII и XVIII веках химикам удалось экспериментально подтвердить эту идею, показав, что некоторые вещества не могут быть подвергнуты дальнейшему расщеплению на составляющие элементы с помощью химических методов. Однако в конце XIX — начале XX века физиками были открыты субатомные частицы и составная структура атома, и стало ясно, что атом не является неделимым.
На международном съезде химиков в Карлсруэ (Германия) в 1860 году были приняты определения понятий молекулы и атома. Атом определён как наименьшая частица химического элемента, входящая в состав простых и сложных веществ.
См. также
Модели атомов
Современная модель атома является развитием планетарной модели. Согласно этой модели, ядро атома состоит из положительно заряженных протонов и незаряженных нейтронов, а вокруг ядра находятся отрицательно заряженные электроны. Однако согласно квантовой механике, электроны не движутся вокруг ядра по определенным траекториям.

Химические свойства атомов
Химические свойства атомов определяются конфигурацией и расположением электронной оболочки. Положение атома в таблице Менделеева определяется электрическим зарядом ядра (числом протонов), в то время как количество нейтронов не влияет на химические свойства. Существует большое разнообразие атомов, и их комбинации в молекулы приводят к образованию огромного количества разнообразных веществ.

Размеры и массы атомов
Атомы имеют микроскопические размеры и массы. Радиусы атомов составляют от 0,046 до 0,25 нм (1 нм = 10^-9 м), при этом самый маленький атом гелия, а самый большой — франция.
Массы атомов также ничтожно малы. Например, масса атома водорода составляет всего 1,67×10^-24 г.
См. также
Заключение
Атомы являются основными строительными блоками вещества. Химические свойства атомов определяются их структурой и конфигурацией электронной оболочки. Разнообразие атомов и их соединений приводит к образованию огромного количества различных веществ. Изучение структуры и свойств атомов позволяет лучше понять мир вокруг нас и применять этот знания в различных областях науки и технологий.

Что нам скажет Википедия?
А́том (от др.-греч. ἄτομος «неделимый[1], неразрезаемый[2]») — частица вещества микроскопических размеров и массы, наименьшая часть химического элемента, являющаяся носителем его химических свойств[1][3].
Атомы состоят из ядра и электронов (точнее, электронного «облака»). Ядро атома состоит из протонов и нейтронов. Количество нейтронов в ядре может быть разным: от нуля до нескольких десятков. Если число электронов совпадает с числом протонов в ядре, то атом в целом оказывается электрически нейтральным. В противном случае он обладает некоторым положительным или отрицательным зарядом и называется ионом[1]. В некоторых случаях под атомами понимают только электронейтральные системы, в которых заряд ядра равен суммарному заряду электронов, тем самым противопоставляя их электрически заряженным ионам[3][4].
Ядро, несущее почти всю (более чем 99,9 %) массу атома, состоит из положительно заряженных протонов и незаряженных нейтронов, связанных между собой при помощи сильного взаимодействия. Атомы классифицируются по количеству протонов и нейтронов в ядре: число протонов Z соответствует порядковому номеру атома в периодической системе Менделеева и определяет его принадлежность к некоторому химическому элементу, а число нейтронов N — определённому изотопу этого элемента. Единственный стабильный атом, не содержащий нейтронов в ядре — лёгкий водород (протий). Число Z также определяет суммарный положительный электрический заряд (Z×e) атомного ядра и число электронов в нейтральном атоме, задающее его размер[5].