В химии существует различие между сильными и слабыми кислотами и основаниями. Понимание этого различия позволяет классифицировать вещества и определить их свойства. В данной статье мы рассмотрим определения, свойства и способы определения сильных и слабых кислот и оснований. Узнайте больше на NOCFN.
Cодержание
Введение
В химии существует различие между сильными и слабыми кислотами и основаниями. Понимание этого различия позволяет классифицировать вещества и определить их свойства. В данной статье мы рассмотрим определения, свойства и способы определения сильных и слабых кислот и оснований.

Определения
Кислота
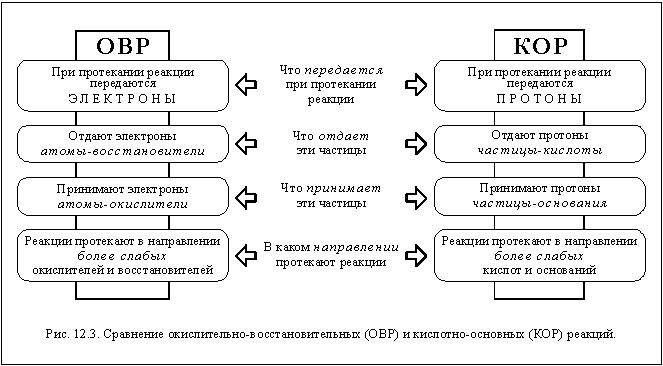
Кислота - это вещество или ион, способные отдавать протоны основанию или другому химическому веществу. Согласно теории Льюиса, кислота может образовывать новое вещество путем обмена электронами с основанием Льюиса. В теории Бренстеда-Лоури кислота определяется как соединение или ион, способные отдать протон.
Основание
Основание - это вещество или ион, способные принять протон от кислоты или другого химического вещества. В теории Льюиса основание может образовывать ковалентную связь с кислотой Льюиса, отдавая пару электронов. В теории Бренстеда-Лоури основание определяется как соединение или ион, способные принять протон.

Свойства кислот и оснований
Свойства кислот
Кислоты обладают следующими общими свойствами:
- Образуют ионы водорода (H+) при диссоциации в растворах или расплавах.
- Могут реагировать с основаниями, образуя новые вещества.
- Могут иметь кислотный вкус, запах и изменять цвет индикаторов в кислых растворах.
Свойства оснований
Основания обладают следующими общими свойствами:
- Могут образовывать ковалентную связь с кислотой Льюиса, отдавая пару электронов.
- Могут принимать протон от кислоты или другого химического вещества.
- Могут иметь щелочной вкус, запах и изменять цвет индикаторов в щелочных растворах.
См. также
Сильные и слабые кислоты и основания
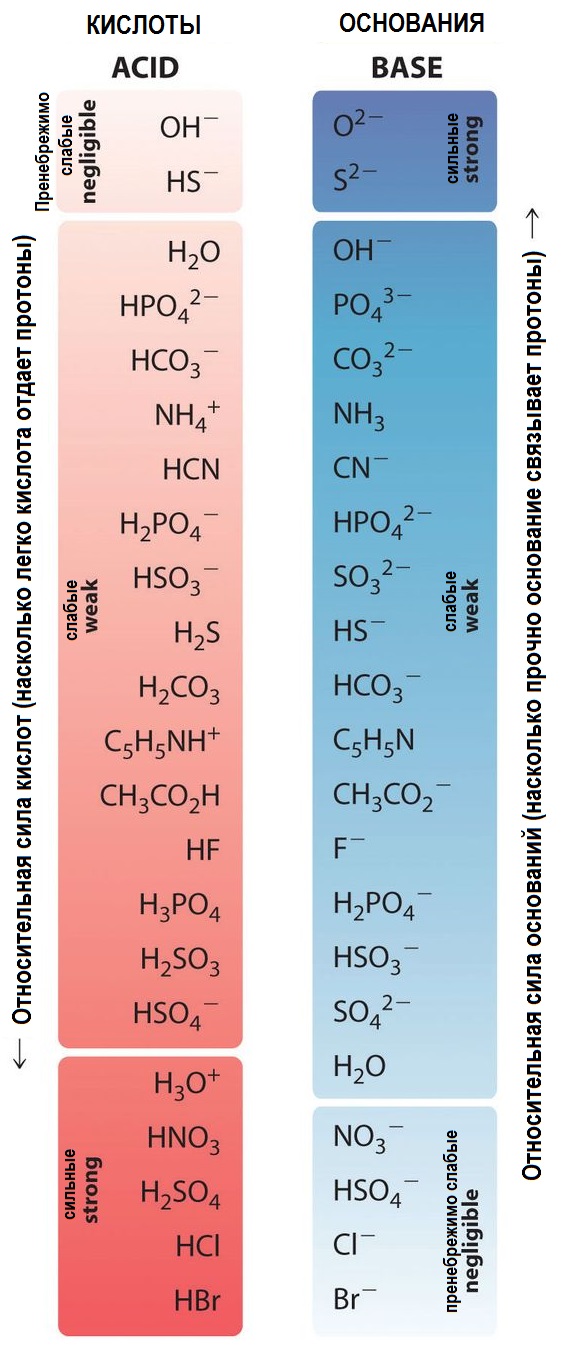
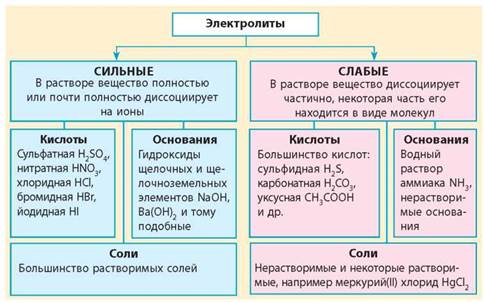
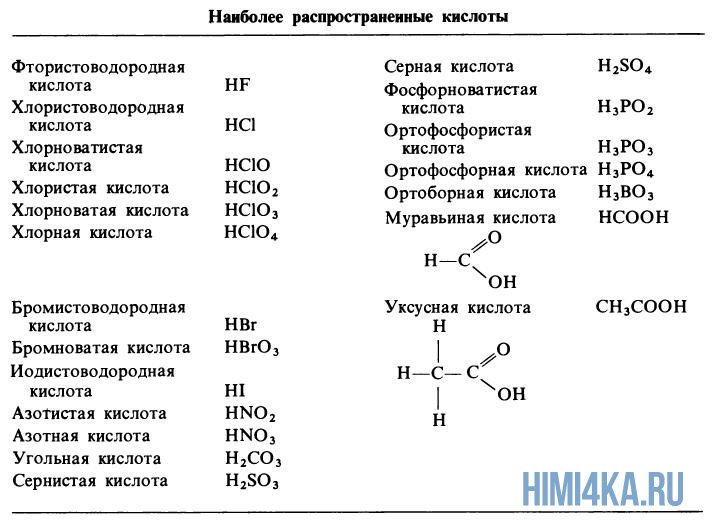
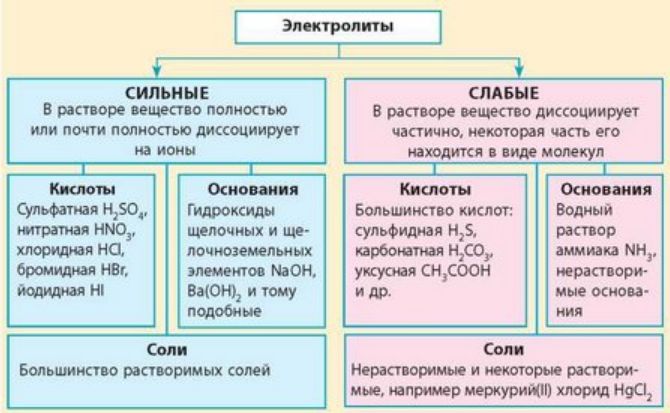
Кислоты и основания могут быть классифицированы как сильные или слабые в зависимости от степени их диссоциации в растворе. Сильные кислоты и основания полностью диссоциируют в растворе, образуя ионы водорода (H+) и анионы или гидроксидные ионы (OH-). Примерами сильных кислот являются соляная кислота (HCl) и серная кислота (H2SO4), а сильным основанием является гидроксид натрия (NaOH).
Слабые кислоты и основания диссоциируются лишь частично, образуя в растворе только небольшое количество ионов. Примерами слабых кислот являются уксусная кислота (CH3COOH) и угольная кислота (H2CO3), а слабым основанием является аммиак (NH3).

Определение pH
pH - это мера кислотности или щелочности водного раствора. Он определяется концентрацией ионов водорода (H+) в растворе. pH меньше 7 указывает на кислотность раствора, pH больше 7 указывает на щелочность раствора, а pH равное 7 указывает на нейтральность.
Существуют различные способы определения pH:
Инструментальный метод
Использование pH-метра - специального прибора, который преобразует концентрацию ионов водорода в электрический сигнал.
Индикаторы
Индикаторы - вещества, которые меняют цвет в зависимости от pH раствора. Используя несколько индикаторов, можно достичь точных результатов измерения pH.

Заключение
Сильные и слабые кислоты и основания отличаются по степени их диссоциации в растворе. Сильные кислоты и основания полностью диссоциируют, в то время как слабые диссоциируют лишь частично. Определение pH позволяет определить кислотность или щелочность раствора. Использование инструментального метода или индикаторов помогает точно измерить pH.